Доставка лікарських засобів всередині організму є складною проблемою. Здавалося б – чого простіше, випив таблетку і чекай, поки подіє. Але таке, системне введення має чимало недоліків – по дорозі до своїх мішеней лікарські речовини взаємодіють із іншими молекулами, послаблюючи або змінюючи свої ефекти, можуть подіяти не туди, внаслідок чого виникнуть небажані побічні ефекти та ін. В ідеалі лікувальні молекули повинні адресно дістатися до певних клітин та діяти там, і тільки там, як це запланували дослідники. Розробка таких засобів триває, і подекуди способи є дуже креативними.
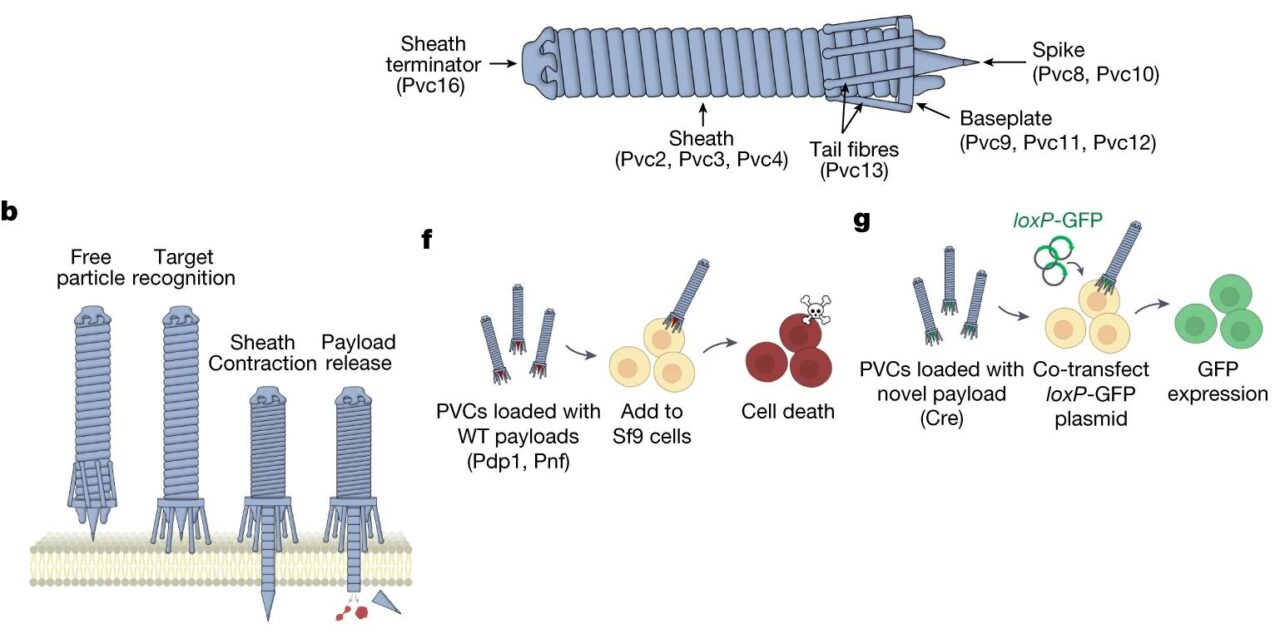
Для розробки одного із них учені використали скоротливу впорскувальну систему (contractile injection system). З шкільного курсу біології ми знаємо бактеріофагів – спеціалізованих вірусів, що мають голівку, трубчастий чохол та “ноги”, якими вони прикріплюються до бактерій. Далі трубка чохла скорочується, внаслідок чого всередину клітини впорскується внутрішній вміст голівки, що містить генетичну інформацію. Подібні системи притаманні і бактеріям, які в такий спосіб атакують еукаріотичні клітини. При цьому вони синтезують шприц-подібні структури, зображені у верхній частині рисунку, та секретують їх за межі своїх клітин. Там ця штука за допомогою основи (baseplate) приєднується до цільової мембрани, проколює її шипом (spike) та, скорочуючи трубку-оболонку (sheath), впорскує в клітину свій вміст.
В якості моделі автори використали “шприци” від Photorhabdus asymbiotica – бактерії, що здатна уражувати клітини як комах, так і людей. Її родичі з роду Photorhabdus є симбіонтами круглих червив, що живляться комахами. Дорослий черв проколює покриви личинок та проникає всередину. Там він випускає бактерій, які починають виробляти токсини, що вбивають личинку за дві доби. Для цього вони використовують описані впорскувальні комплекси (як це показано на рисунку в частині f). Живлячись вбитими клітинами, бактерії перетворюють їх на поживне для черва середовище. Коли ж личинку доїли, дорослі нематоди покидають оболонку та шукають нову жертву. Такий от мутуалізм.
Високу інсектицидну ефективність Photorhabdus людина навчилася ефективно використовувати проти комах-шкідників. Тут бактерій використовують без їхніх нематод-симбіонтів.
На відміну від родичів, Photorhabdus asymbiotica здатна рости за порівняно високих температур (37 °C), що і обумовлює її здатність успішно заражати людину. Патогенні молекулярні агенти, що їх переносять ці бактерії споріднюють їх із сальмонелами та єрсиніями (збудниками чуми). Такі обумовлені Photorhabdus asymbiotica інфекції трапляються переважно в США, Австралії, Таїланді, Непалі та у деяких країнах Європи.
В результаті дослідження учені зробили дві ключові речі. По-перше, використавши методи молекулярного моделювання, вони змінили структуру білків “шприців” так, що ті уражали лише клітини, які мали на своїй поверхні специфічні молекулярні мітки. Це дозволило доставляти корисний вміст виключно у клітини певного типу – наприклад, нейрони. Якщо ми знаємо молекулярний профіль потрібних клітин, то зможемо високо селективно впливати, наприклад, на ракові клітини, що відмінні від здорових. Крім того, дослід показав, що впорскувачі можна запрограмувати на чужі для них клітини (мишачі). По-друге, дослідникам вдалося замінити природний вміст “шприців” на інші молекули, які можуть бути корисними людині. І тут відкриваються чималі перспективи, адже такими сполуками можуть бути редактори ДНК (Cas9 або модифікатори основ) або ж специфічні токсини.
Отже, розроблений спосіб програмованої доставки молекул має перспективи у генній терапії, лікуванні онкології, біологічному контролі шкідників тощо.
Джерело: Kreitz J, Friedrich MJ, Guru A, Lash B, Saito M, Macrae RK, Zhang F. Programmable protein delivery with a bacterial contractile injection system. Nature. 2023 Apr;616(7956):357-364. doi: 10.1038/s41586-023-05870-7
Залишити відповідь